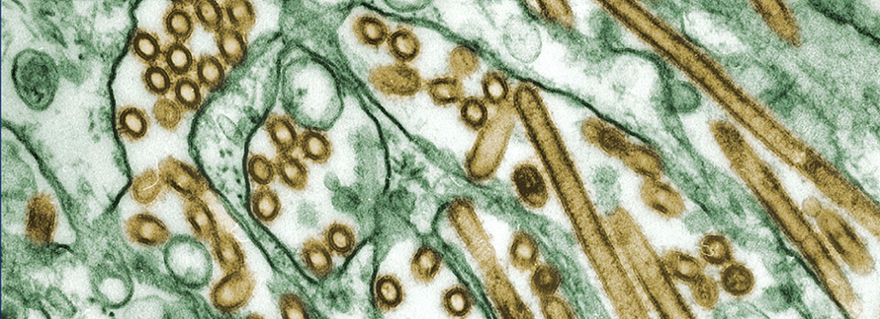
Veelzijdige antivirus-eiwitten ontdekt met computerkracht
Eén klein molecuul dat zowel griep-, corona-, hiv- en zika-virussen kan vernietigen: het bestaat. Een algoritme dat de evolutie nabootst, leverde eiwitmoleculen op die in het laboratorium werken tegen zika en hiv. Biofysicus Niek van Hilten droeg eraan bij, hij promoveerde cum laude op 14 september.
Virusvaccins en virusremmers lopen tegen twee problemen aan. Tegen elk virus is een specifiek middel nodig en dat werkt maar tijdelijk, omdat virussen snel evolueren. Bijna alle middelen richten zich op eiwitten die als vlaggetjes uit het virus steken. Niek van Hilten: ‘Dat is historisch zo gegroeid, bijna alle medicijnen doen dat. Maar elk virus heeft unieke eiwitten en die veranderen steeds.’
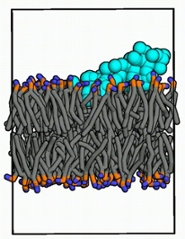
Molecuul dat de kromming aanvoelt
Biofysicus Van Hilten werkte mee aan onderzoek naar virusmedicijnen met een heel andere aanvalsmethode. ‘Veel virussen hebben de vorm van kleine bolletjes. Corona, griep, hiv en zika bijvoorbeeld, zijn zulke enveloped virusses. Ze zijn bijna duizend keer zo klein als onze eigen cellen.’ Ze hebben net zo’n membraan als menselijke cellen: een dubbele laag vetmoleculen met de lange staarten naar elkaar toegekeerd (zie afbeelding). ‘Omdat virussen zo klein zijn, is hun membraan veel meer gekromd dan dat van onze lichaamscellen. Sommige kleine eiwitten kunnen die kromming aanvoelen, vervolgens het membraan doorboren en zo het virus vernietigen.’
Dat er eiwitten bestaan die bolletjesvirussen zo kunnen bestrijden, is al twintig jaar geleden ontdekt. ‘Toen bleek een eiwitmolecuul genaamd “AH” envelop-virussen te herkennen aan hun membraan en dat vervolgens te perforeren . Fataal voor het virus.’ Onderzoekers testten al verschillende varianten op muizen en makaken.
From scratch ontwerpen om het precies te begrijpen
Een revolutionair virusmedicijn lijkt dichtbij, als het onderzoek al in het stadium van apenstudies is. Toch leert de ervaring dat er nog veel mis kan gaan op de resterende lange weg naar ingebruikname ervan, aldus Van Hilten. Mede daarom is het onderzoek van hem en zijn collega’s belangrijk. ‘Wij gebruiken het AH-eiwit als voorbeeld om precies te begrijpen hoe zo’n medicijn werkt en om zo’n eiwit from scratch te ontwerpen.’ Dat is gelukt.
De eiwitmoleculen die virusmembranen herkennen, bestaan uit 24 blokjes van één aminozuur. Van Hilten: ‘Er bestaan twintig verschillende aminozuren, Dat betekent dat er 2024 mogelijkheden zijn om een eiwit van 24 blokjes te bouwen. Dat zijn er ongeveer 17 met 30 nullen.’ Te veel om virtueel te testen, zelfs voor een algoritme dat met supercomputerkracht kan rekenen.
Eiwit-evolutie door een algoritme
Collega-promovendus Jeroen Methorst schreef daarom een evolutionair algoritme dat met 144 willekeurige mogelijke eiwitten startte. ‘Dat is het efficiëntste aantal dat de rekenkracht van onze supercomputers aankon.’ Het algoritme checkte in een virtueel stukje membraan dat Van Hilten ontwikkelde, hoe goed deze eiwitten een krom virusmembraan zouden kunnen onderscheiden en perforeren. Daarna liet het de beste exemplaren zich met elkaar voortplanten. ‘Na 25 generaties gingen de prestaties van de moleculen niet meer omhoog en stopten we.’
In Leiden en in het Duitse Ulm synthetiseerden collega-onderzoekers enkele veelbelovende varianten. ‘Bij laboratoriumtest bleken sommige van deze eiwitten te werken tegen zika en hiv, en ze waren veilig voor menselijke celmembranen. Toen ik dat hoorde… Dat was het mooiste moment van mijn promotieonderzoek.’
Filmpje van moleculen helpt onderzoekers
Een vernieuwend aspect aan het algoritme waarmee de onderzoekers werkten, is de combinatie van een evolutionair algoritme en simulaties van moleculaire dynamica. Van Hilten: ‘Dat laatste is een techniek om de bewegingen en interacties van moleculen te simuleren. Het resultaat is een filmpje (zie onderstaande video, red) waarop je ziet wat de moleculen doen. Veel andere algoritmen werken als een black box en spugen een resultaat uit, bij ons algoritme kon je van elke uitkomst zien wat het deed.’ Van Hilten zorgde dat moleculaire dynamica in het algoritme kon worden geïntegreerd. ‘Daarmee kunnen we zulke algoritmen ook allerlei andere ontwikkelvragen stellen, waarbij je vervolgens kunt zien wat de resulterende moleculen doen.'
De bewegingen en interacties van moleculen
Vanwege de gekozen cookie-instellingen kunnen we deze video hier niet tonen.
Bekijk de video op de oorspronkelijke website ofVan Hilten laat bij zijn vertrek naar San Francisco voor een postdoc-functie zijn collega’s achter met mooie nieuwe mogelijkheden, maar ook met nieuwe vragen. ‘Waarom werkten niet alle moleculen die het algoritme had voorgesteld? Waarschijnlijk omdat ons model nog heel simpel was. Het algoritme keek bijvoorbeeld alleen naar het gedrag van de eiwitten in heel eenvoudige membranen, gemaakt van één soort vetmoleculen. In de biologische realiteit zijn het wel vijftig verschillende.’
Tekst: Rianne Lindhout
