
LUMC gaat eerste Nederlandse stamcelgentherapie toedienen aan patiënten
Artsen en onderzoekers van het Leids Universitair Medisch Centrum (LUMC) starten met een klinische studie, waarbij zij de allereerste stamcelgentherapie in Nederland gaan toedienen. De stamcelgentherapie is bedoeld als behandeling voor kinderen die geboren worden met de zeldzame ziekte SCID, waardoor zij geen eigen immuunsysteem hebben.
'Wij zijn de eerste ter wereld die stamcelgentherapie hebben ontwikkeld voor deze vorm van SCID, RAG1-SCID om precies te zijn. Daarnaast is het de eerste door Nederland geïnitieerde stamcelgentherapie die ook daadwerkelijk wordt toegepast in patiënten,' vertelt hoogleraar Stamcelbiologie Frank Staal. De onderzoekers zijn in totaal 15 jaar bezig geweest om de therapie te ontwikkelen. Dat ze nu de klinische studie kunnen openstellen voor patiënten, noemt hij een mijlpaal. 'We kunnen eindelijk van start en onze eerste patiënten behandelen. Omdat het een zeer zeldzame aandoening is bij pasgeborenen, moet de eerste patiënt die mee kan doen aan de studie waarschijnlijk nog geboren worden,' zegt Staal.
De juiste donor
Severe Combined Immunodeficiency (SCID) is een zeldzame aangeboren afweerziekte. Kinderen met SCID worden geboren zonder essentiële afweercellen waardoor zelfs een onschuldig verkoudheidsvirus al fataal kan zijn. Zonder een stamceltransplantatie overlijden de patiënten voor hun eerste levensjaar. 'Als er een stamceldonor wordt gevonden waarvan de weefseltypering (HLA) overeenkomt met dat van de patiënt, is de kans op genezing zeer hoog, wel 80 tot 90%,' legt Arjan Lankester, hoogleraar Kindergeneeskunde en Stamceltransplantatie bij het Willem-Alexander Kinderziekenhuis, uit.
Voor de helft van de patiënten is er helaas geen goed passende donor beschikbaar. 'Omdat stamceltransplantatie de enige kans op overleving is, moeten we regelmatig gebruik maken van een donor waarvan de weefseltypering maar voor een gedeelte overeenkomt met die van de patiënt. De kans op overleving ligt in dit geval zo’n 20% lager en ook de kwaliteit van leven na transplantatie is minder,' vervolgt Lankester. Daarnaast gaat iedere stamceltransplantatie gepaard met een risico op een ongewenste reactie van de donorcellen tegen het lichaam van de patiënt, zogenoemde graft-versus-host ziekte.
Je eigen donor
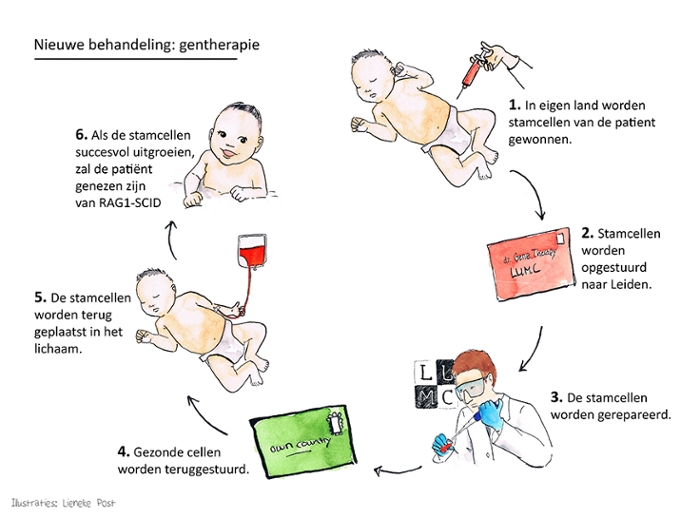
'Met stamcelgentherapie kunnen we deze problemen oplossen. De patiënten zijn bij deze therapie namelijk hun eigen donor,' legt Staal uit. 'De fout die in de stamcellen van de patiënt aanwezig is wordt in ons laboratorium gecorrigeerd. We doen dit met een kreupel gemaakt virus dat een goede versie van het gen inbouwt in het DNA van de stamcellen. Vervolgens geven we de gecorrigeerde stamcellen weer terug aan de patiënt. Uit deze cellen kan dan een goed werkend immuunsysteem groeien. We pakken het probleem dus echt bij de bron aan,' vertelt Staal.
Zo makkelijk als het misschien klinkt, zo moeilijk bleek dat in de praktijk. Staal: “We zijn er niet voor niets bijna 15 jaar mee bezig geweest. De vorm van SCID waar wij ons op richten wordt veroorzaakt door mutaties in een heel lastig gen, RAG1. We hebben allerlei trucjes moeten uithalen om het te laten slagen. Des te blijer zijn we nu dat het gelukt is.' Met deze Leidse doorbraak is stamcelgentherapie nu voor de derde genetische vorm van SCID beschikbaar. Hierdoor kan deze therapie uiteindelijk voor het merendeel van alle toekomstige SCID-patiënten uitkomst bieden.
Cellen reizen, patiënt niet
Tijdens de ontwikkeling van deze nieuwe therapie zijn Staal en Lankester samenwerkingen aangegaan met topinstellingen uit andere Europese landen. 'Hierdoor konden we niet alleen onze ervaringen delen, maar ook een unieke structuur opzetten die de patiënt met deze zeldzame ziekte ten goede komt,' zegt Lankester. Waar SCID-patiënten en hun ouders voor de twee bestaande stamcelgentherapieën meerdere maanden in Milaan, Londen of Parijs moeten verblijven, kan de gentherapie voor RAG1-SCID vanuit het LUMC in meerdere Europese landen beschikbaar worden gesteld.
Het motto van Staal en Lankester luidt dan ook: de cellen reizen, niet de patiënt. Lankester: 'In onze studie zullen stamcellen van buitenlandse patiënten worden afgenomen in het eigen ziekenhuis, waarna de cellen in ons laboratorium worden bewerkt en vervolgens teruggestuurd naar de Europese partnerziekenhuizen.' Hierdoor kan het gezin in hun vertrouwde omgeving blijven, wat vanzelfsprekend grote voordelen heeft. Ook zal deze organisatiestructuur de therapie voor meer Europese patiënten toegankelijk maken.
Unieke setting
Het feit dat het LUMC als eerste academische instelling in Nederland stamcelgentherapie heeft ontwikkeld tot klinische toepassing, komt volgens Staal en Lankester door de goede samenwerking tussen afdelingen. 'Het LUMC biedt een fantastische setting waar alle expertises, van onderzoekers tot artsen en farmacologen, samenkomen. Dat is een van de belangrijkste redenen waarom het ons gelukt is om deze therapie te ontwikkelen,' vertelt Lankester. 'Deze nieuwe therapie bouwt voort op de lange historie die het LUMC heeft met de behandeling van patiënten met aangeboren afweerziekten. Meer dan vijftig jaar geleden werd de eerste succesvolle Europese stamceltransplantatie bij een patiënt met SCID uitgevoerd in het LUMC.'
Breder toepasbaar
De onderzoekers zijn er van overtuigd dat deze technologie ook gebruikt kan worden voor andere zeldzame aandoeningen. 'Uiteraard is elk gen weer anders,' zegt Staal. 'We doen nu ook onderzoek naar een ander SCID-gen, namelijk RAG2, en dat blijkt toch weer om een andere aanpak te vragen. Maar ik heb er alle vertrouwen in dat we dit verder kunnen ontwikkelen tot een veelzijdig toepasbare therapie voor een groot aantal aandoeningen, waaronder andere afweer- en stofwisselingsziekten waarvoor nu nog geen optimale behandelopties beschikbaar zijn.'
